01
2D细胞培养的局限性
细胞培养开始于 19 世纪末,在过去一个世纪中,维持和分析贴壁细胞系最流行的方法是 2D 或单层培养,但科学家们一直试图解决一个问题,如何让细胞在体外活的更真实呢?2D细胞培养像是“细胞住平板房”(图1),但真实的人体是“细胞住立体社区”(图2) ,而细胞3D培养是一种将细胞在三维空间进行培养的技术,能更好的在体外模拟体内环境,弥补了传统2D细胞培养的不足。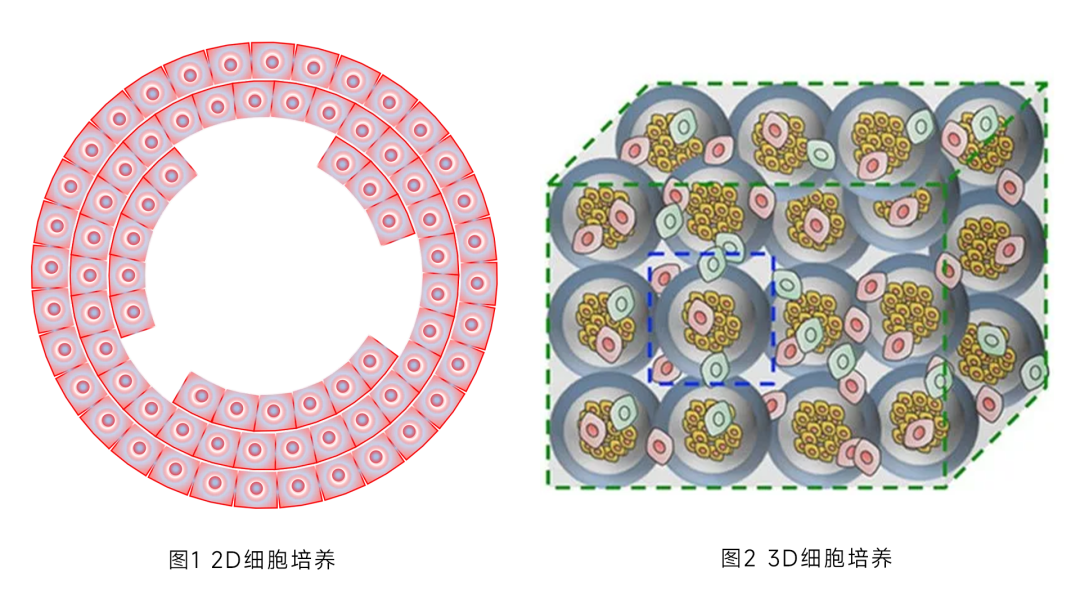
细胞形态和功能受限
细胞与微环境交互不足
2D培养中细胞对培养基中营养物质和生长因子的摄取方式与体内不同,所有细胞接收到的营养和因子基本相同,缺乏体内复杂的化学梯度。细胞与细胞外基质(ECM) 的相互作用也被简化,无法体现体内细胞与 ECM 离散连接的特点,影响细胞的信号传导、增殖和分化等过程。
实验结果与体内情况差异大
模拟体内真实环境
体内细胞处于复杂的三维环境中,与周围细胞和 ECM 紧密相互作用。3D 培养能够更好地模拟这种环境,使细胞呈现自然的形态和极性,有利于细胞间的信号传导和物质交换,更准确地反映细胞在体内的行为和功能,如细胞的增殖、分化、迁移等过程。
提高实验准确性
在药物研发、疾病研究等领域,3D 培养的细胞对药物的反应更接近体内情况,能够提供更可靠的实验数据。通过 3D 培养可以更准确地评估药物的疗效和毒性,减少动物实验的需求,提高研究效率和成功率。
深入研究细胞行为和疾病机制
3D 培养有助于研究细胞在复杂环境中的行为,如肿瘤细胞的侵袭和转移、干细胞的分化调控等。对于理解疾病的发生、发展机制,以及开发新的治疗方法具有重要意义。
微流控概念
微流控是一种操控微小体积流体的技术,它能够在微观尺度上精确控制流体的流动、混合、分配等行为。通过在芯片上构建微小的通道、阀门、反应室等结构,实现对生物、化学等过程的精确控制和分析。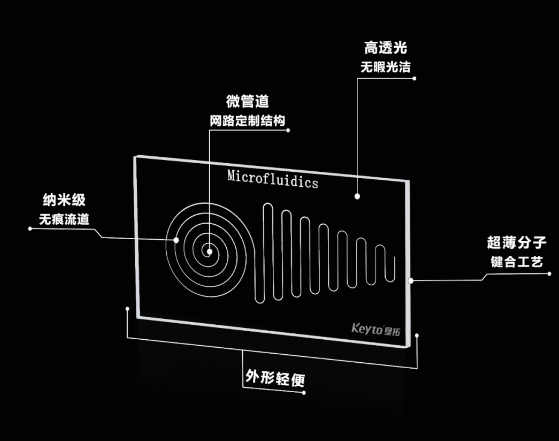
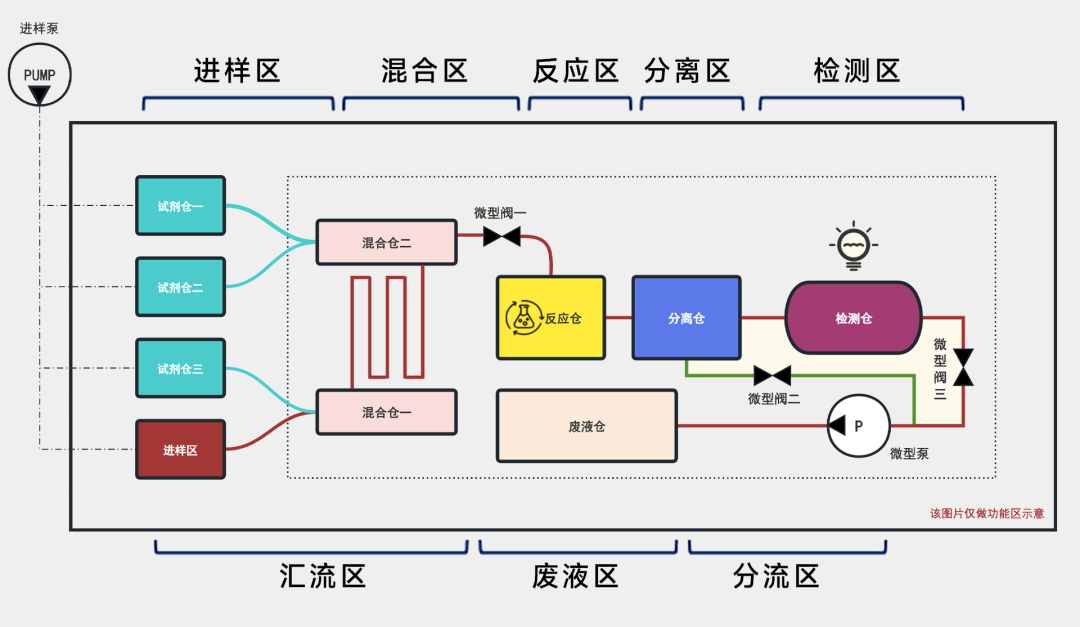
微流控技术具有体积小、消耗低、通量高、可集成化等优点,在生物医学、化学分析等领域有广泛应用。在细胞培养方面,微流控系统可以为细胞提供更接近体内的微环境,实现对细胞生长、分化、相互作用等过程的精确调控和监测。
精确控制微环境
微流控系统可以精确调控细胞培养的微环境,如通过控制流体流动来调节营养物质、生长因子的浓度和分布,模拟体内的化学梯度。还能调节微环境的物理参数,如剪切应力、基质刚度等,为 3D 培养的细胞提供更接近体内的生长条件。
实现高通量和自动化
微流控技术适合高通量实验,能够同时培养多个样本,提高实验效率。结合自动化设备(图3),可以实现细胞接种、培养基更换、数据采集等过程的自动化,减少人为误差,提高实验的可重复性和可靠性。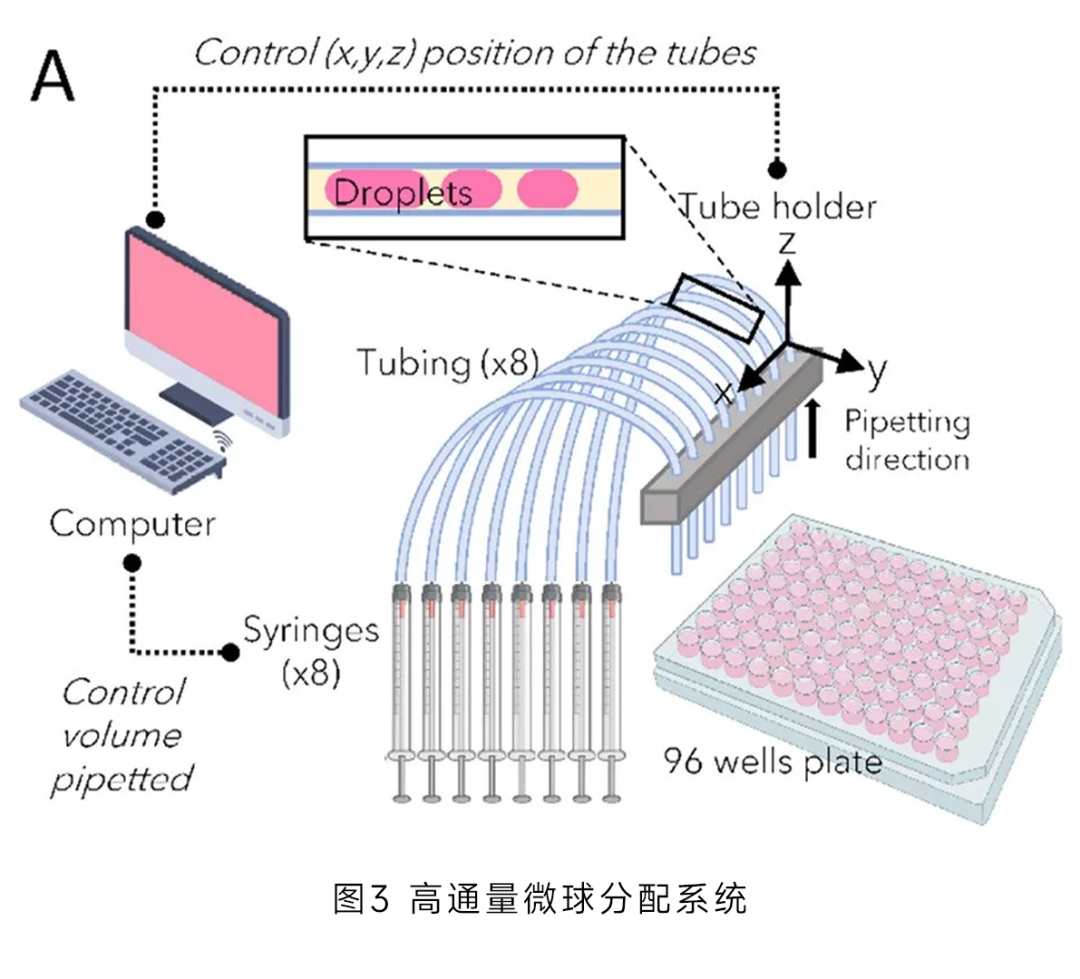
便于集成检测和分析
微流控芯片可以集成多种检测和分析功能(图4),如光学检测、电化学检测等,能够实时、原位地监测细胞的生长状态、代谢活动、基因表达等指标,为 3D 细胞培养提供丰富的信息,有助于深入了解细胞的行为和功能。

04
微流控在细胞3D培养中的案例
微球封装细胞
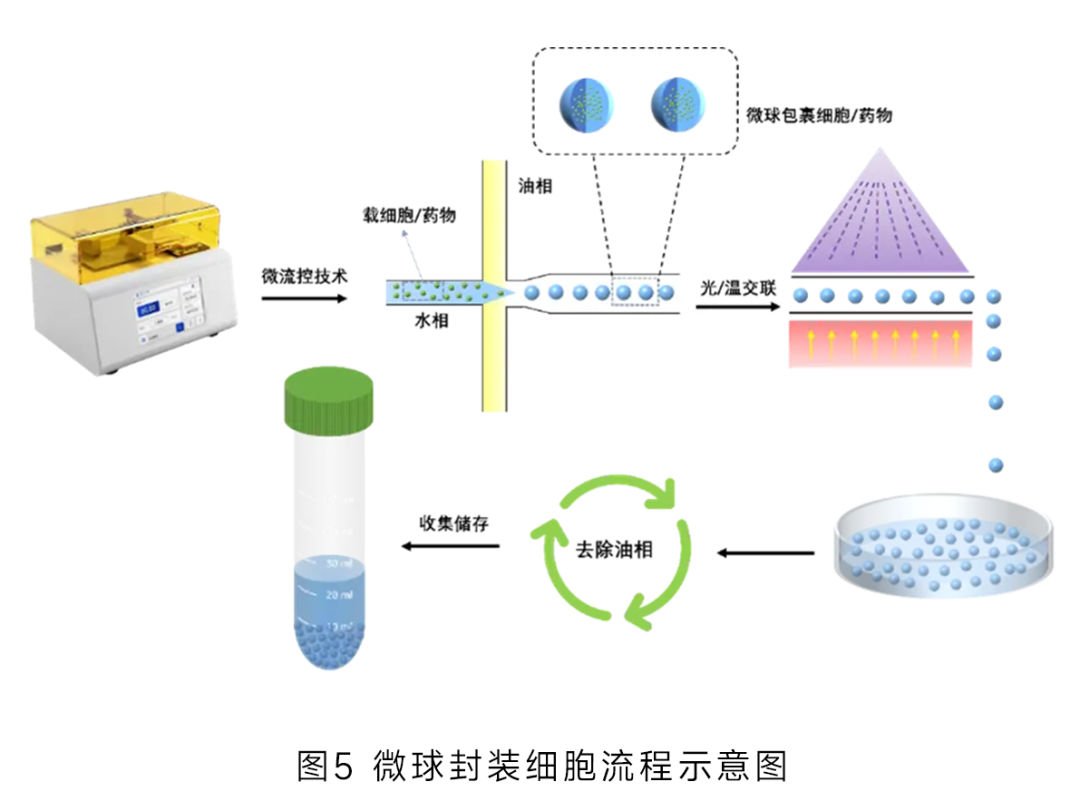
基于微流控芯片内部的微通道网络,利用流体力学原理,将含有细胞的生物溶液与用于形成微球的材料溶液(如聚合物溶液、水凝胶)在微通道中精确操控和混合。通过调节微通道的尺寸、流体流速等参数,使两种溶液在特定位置形成微小的液滴或微球结构,细胞被包裹在这些微球内部,随后经过物理或化学方法使微球固化成型,从而实现细胞的稳定包裹 (图5)。
疾病模型构建
在肿瘤研究领域,深入探究肿瘤侵蚀血管的机制至关重要,它对于理解肿瘤转移和开发有效的抗癌疗法意义重大。
微流控技术作为一种前沿技术,能够在微小的通道内精确操控流体,为模拟生物体内微环境提供了有力手段;而血管化芯片则可构建出具有血管结构的微环境(图6)。将两者结合用于研究肿瘤侵蚀血管时,首先在微流控芯片上精心构建出包含血管结构的三维微环境,通过精确控制流体,模拟体内血液循环。接着将肿瘤细胞引入该微环境中,观察肿瘤细胞在血管化芯片上的生长、迁移以及与血管相互作用的过程(图7)。
研究人员能够实时监测肿瘤细胞如何突破血管壁、侵入血管内部,分析其侵蚀血管的分子机制和影响因素。这一研究方法不仅克服了传统研究模型的局限性,还能在微观层面为肿瘤侵蚀血管的研究提供更精准、更详细的数据,有助于推动肿瘤治疗领域的新突破。

器官模型构建
微流控技术能在微小通道内精确操控流体,皮肤器官芯片则模拟了人体皮肤的结构和功能,二者结合为皮肤研究带来了革新。欧莱雅已成功运用这一技术组合,用皮肤芯片替代动物测试。
在这一应用中,微流控技术精准控制营养物质、药物等流体在皮肤器官芯片中的输送,模拟皮肤在不同环境下的生理状态。
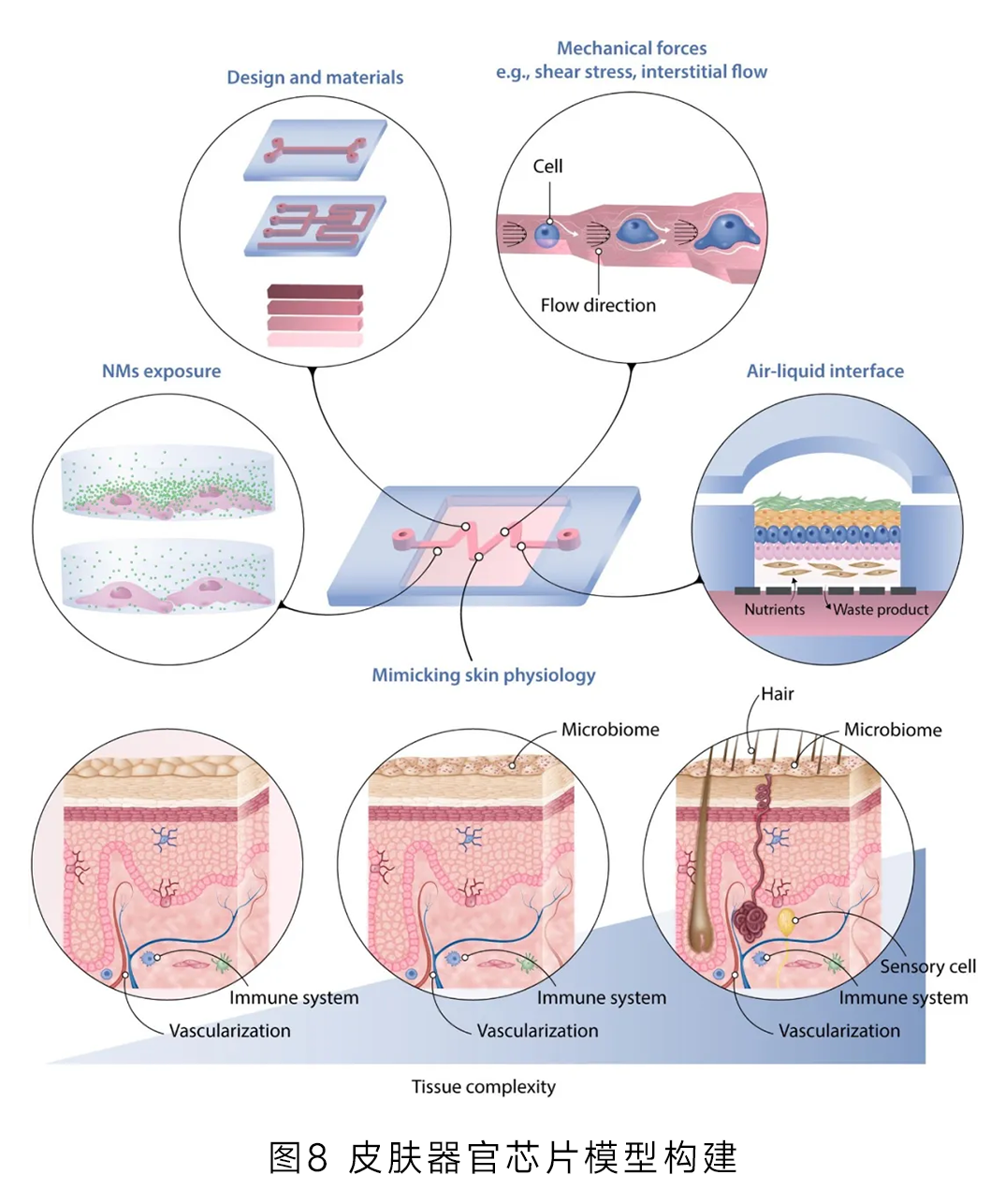
皮肤器官芯片由多种细胞和细胞外基质构建,高度还原真实皮肤组织(图8);这一替代不仅避免了动物实验伦理争议,还提供了更精准、更具生理相关性的测试结果,以更科学、更人道的方式评估产品功效与安全性,推动行业朝着绿色、可持续方向发展。
05
在生命科学快速发展的时代,微流控与细胞3D培养的结合展现出极为广阔的前景。未来,随着技术的不断创新,二者融合有望在医学领域实现重大突破,例如构建高度仿真的人体器官模型,助力疾病机制的深入研究,为个性化医疗方案的制定提供精准依据。

在制药行业,能够更高效地筛选和评估药物,极大缩短新药研发周期,降低研发成本。在组织工程方面,可制造出具有复杂结构和功能的人造组织与器官,缓解器官移植供体短缺的困境。
此外,随着微流控技术在微尺度操控上的进一步优化,细胞3D培养体系的不断完善,二者的结合将在生物传感器开发、再生医学等新兴领域持续拓展,为解决人类健康问题带来更多可能,推动整个生命科学领域迈向新的高度。

