
材料: 常用材料包括硅、玻璃、聚合物(如PDMS、PMMA、PC)和纸基材料。选择取决于应用需求(如光学透明度、生物相容性、成本、加工难易度)。
痛点解决: 替代宏大的试管、烧杯和连接管路,极大减少样品和试剂消耗(微升至纳升级),显著缩短扩散距离和反应时间,提高反应效率和分析速度。

结构与功能: 提供流体流动所需的动力,并精确控制流速、流向和时序。
常见方式包括:
微泵:产生流体驱动力;
微阀:控制流体的通断、切换和分配;
驱动源: 外部压力源(注射泵、真空泵)、电场(电渗流)、离心力场、毛细力等。
注:垦拓支持阀泵模块及系统集成定制。
痛点解决:实现流体操控的自动化与程序化,减少人工操作步骤和人为误差,提供高度可重复的流体控制,为复杂多步反应集成提供基础。

结构与功能: 在微型空间里,流体通常呈层流状态,分子扩散是主要混合机制,速度慢。微混合器设计特殊结构(如蛇形通道、障碍物、混沌对流结构、声波/电动力扰动)来增强混合效果。
痛点解决:加速试剂与样品的混合,确保反应的均一性和充分性,克服微尺度层流导致的混合困难,提升反应效率和检测灵敏度。
结构与功能: 芯片上设计的特定区域,用于容纳流体进行孵育、化学反应、类器官、细胞培养、核酸扩增(如微流控PCR)等。其形状、体积和表面性质可根据特定反应优化。
痛点解决:提供受控的微反应环境(温度、时间),精确控制反应物浓度和体积,实现高通量并行反应(多腔室阵列),特别适合珍贵/微量样品分析。

结构与功能: 用于在芯片上分离不同组分(如细胞、蛋白质、DNA片段)。
常见技术包括:
微电泳: 利用电场分离带电分子。
微色谱: 在微通道内填充或修饰固定相进行分离。
介电泳: 利用非均匀电场分离颗粒/细胞。
确定性侧向位移: 利用微柱阵列按大小分离细胞/颗粒。
过滤结构: 物理筛分。
痛点解决:将分离步骤集成到芯片上,减少样品转移损失和污染风险,实现快速、高效的组分分离和富集,提高后续检测的灵敏度和特异性。
结构与功能: 集成在芯片上或与芯片联用的器件,用于实时或终点检测反应结果。
常用方法包括:
光学检测: 荧光、吸光度、化学发光、表面等离子体共振(SPR)。常需集成波导、透镜或直接利用显微镜/CCD。
电化学检测: 安培法、伏安法、阻抗谱。集成微电极进行检测。
质谱接口: 将芯片流出物导入质谱仪。
痛点解决:实现原位、实时检测,提高检测通量和速度,减少样品处理步骤,降低检测下限(因检测体积小、信号富集),推动便携式、即时检测设备的发展。
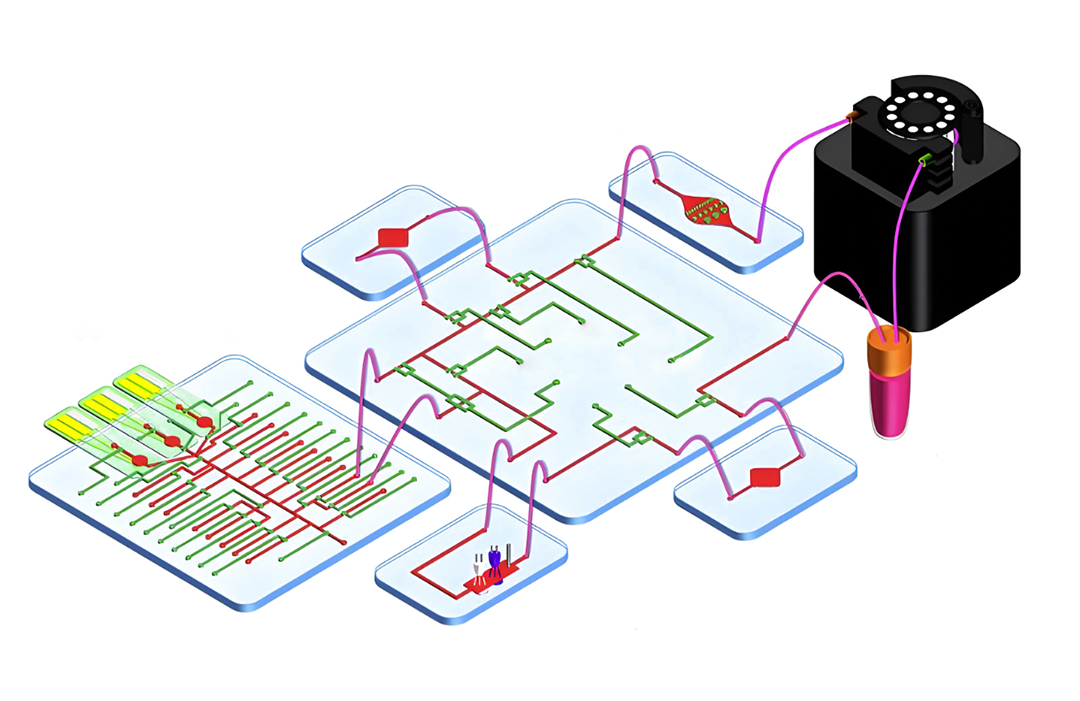
结构与功能: 包括流体接口(连接外部泵、阀、样品/试剂储液池和废液池)和电学接口(连接外部电极、检测器、控制器)。设计需保证密封性、低死体积和易操作性(如标准接口、穿刺式接口)。
痛点解决:实现芯片与宏观世界的可靠连接,确保流体和信号的稳定输入输出,影响系统的易用性和可靠性。

微流控芯片的价值,正是源于其解决传统实验室痛点的强大能力:
痛点:珍贵样本消耗殆尽? 微流控:纳升消耗,让微量样本分析成为可能。
痛点:昂贵试剂成本高昂? 微流控:微量试剂,大幅降低实验成本。
痛点:实验流程漫长? 微流控:高效混合与传质,集成化流程,显著缩短分析时间(分钟级 vs 小时/天级)。
痛点:操作繁琐易错? 微流控:自动化操控,减少人工干预,提高实验重复性和准确性。
痛点:大型设备不便携? 微流控:芯片小型化,为开发便携式、床旁诊断设备奠定基础。
痛点:高通量分析困难? 微流控:易于并行化(多通道/腔室阵列),实现高通量筛选与分析。
痛点:多步骤操作样本易损失污染? 微流控:集成“样品进-结果出”,封闭系统减少损失与污染风险。